
Revista Portuguesa de Estomatologia, Medicina Dentária e Cirurgia Maxilofacial
SPEMD - Rev Port Estomatol Med Dent Cir Maxilofac | 2018 | 59 (4) | 191-197
Investigação Original
Efeito anti-placa de bochechos no crescimento de placa bacteriana supra-gengival: um ensaio clínico aleatório
Antiplaque efficacy of mouthwashes on 3-day supragingival plaque regrowth: a randomized crossover clinical trial
a Faculdade de Medicina Dentária da Universidade de Lisboa
b ciTechCare – Center for Innovative Care and Health Technology, Polytechnic Institute of Leiria
Henrique Luís - enrique.luis@fmd.ulisboa.ptenrique.luis@fmd.ulisboa.pt
Article Info
Rev Port Estomatol Med Dent Cir Maxilofac
Volume - 59
Issue - 4
Investigação Original
Pages - 191-197
Go to Volume
Article History
Received on 27/09/2018
Accepted on 28/12/2018
Available Online on 29/01/2019
Keywords
Investigação original
Efeito anti-placa de bochechos no crescimento de placa bacteriana supra-gengival: um ensaio clínico aleatório
Antiplaque efficacy of mouthwashes on 3-day supragingival plaque regrowth: a randomized crossover clinical trial
Giovanna S.C. Tarlattinia, Sandra Ribeiroa, Teresa Albuquerquea, Henrique Luísa,b,*
a Faculdade de Medicina Dentária da Universidade de Lisboa
b ciTechCare – Center for Innovative Care and Health Technology, Polytechnic Institute of Leiria
http://doi.org/10.24873/j.rpemd.2018.11.418
Resumo
Objetivo: O objetivo deste estudo foi o de avaliar o efeito antiplaca de um bochecho com óleos essenciais (EO) sem álcool e de um bochecho de cloreto de cetilpiridínio (CPC) em comparação com um controlo positivo de clorohexidina (CHX), utilizando um modelo in vivo de crescimento de placa bacteriana durante três dias.
Métodos: Este estudo foi desenvolvido como um ensaio clínico cruzado, cego e aleatorizado, que envolveu 16 voluntários. Após receberem a profilaxia profissional, durante os três dias seguintes, cada voluntário deixou de utilizar qualquer outro meio de higiene oral e realizou dois bochechos diários com 20 ml de um dos colutórios em teste. O bochecho de clorohexidina a 0,2% foi utilizado como controlo positivo. Após os três dias, o índice de placa foi avaliado e os participantes preencheram um questionário para manifestar a opinião em relação ao produto utilizado. Cada voluntário passou por um período de washout de 14 dias entre cada fase do estudo.
Resultados: O grupo que utilizou o CPC mostrou um melhor efeito na inibição do crescimento da placa bacteriana, quando comparado com o grupo EO. De facto, a média global do índice de placa bacteriana foi menor com a utilização do CPC (1,30) do que com o uso do EO (1,73) e da CHX (1,54). Todos estes valores foram estatisticamente significativos (P<0,031).
Conclusão: O CPC apresentou melhores resultados na redução da placa bacteriana quando comparado com o EO e com a CHX.
Palavras-chave: Cloreto de cetilpiridínio,Clorhexidina,Colutórios, Óleo essencial, Placa bacteriana,Sem álcool
Abstract
Objective: The aim of this study was to evaluate the antiplaque effects of an alcohol-free essential-oil (EO) mouthwash and a cetylpyridinium chloride (CPC) mouthwash compared to a chlorhexidine (CHX) mouthwash as a positive control, using an in-vivo plaque regrowth model of 3 days.
Methods: The study was designed as a masked, randomized, crossover clinical trial, involving 16 volunteers. After receiving thorough professional prophylaxis at baseline, over the next 3 days, each volunteer refrained from all other oral hygiene measures and performed two daily rinses with 20 ml of the test mouthwashes. A 0.20% chlorhexidine rinse served as a positive control. After 3 days, the plaque index was evaluated, and the participants answered a questionnaire on their opinion about the product used. Each subject underwent a 14-day washout period and, then, there was another allocation.
Results: The CPC group showed a better effect on the inhibition of plaque growth than the EO group. In fact, the overall mean plaque index was lower with CPC (1.30) than with EO (1.73) and CHX (1.54). All these values were statistically significant (P<0.031).
Conclusion: The CPC had better results in reducing bacterial plaque than EO and CHX.
Keywords: Cetylpyridinium chloride,Chlorhexidine,Mouthwashes, Essential oils, Dental plaque,Alcohol free
Introdução
A cavidade oral possui características de humidade e temperatura ideais para o desenvolvimento bacteriano, constituindo um ecossistema com diversas espécies. Algumas destas encontram‑se organizadas sob a forma de um biofilme e possuem a capacidade de colonizar as superfícies dentárias.1 A acumulação de microrganismos, sobre as superfícies duras da cavidade oral, é considerada o principal motivo para a presença de cárie dentária, gengivite, periodontite, infeções perimplantares e estomatites. Como forma de prevenção destas doenças orais é necessário manter uma boa higiene oral através de medidas regulares de remoção do biofilme. Estas podem ser mecânicas, químicas ou a associação de ambas. 2, 3
A clorohexidina (CHX) é o antisséptico mais estudado e mais eficaz na inibição da placa bacteriana e na prevenção da gengivite.4 A sua efetividade está relacionada com a sua actividade bactericida, em altas concentrações, bacteriostática, em baixas concentrações, e ao facto de ter uma elevada substantividade na cavidade oral: 12 horas.5 Apesar dos seus efeitos benéficos, a clorohexidina pode apresentar alguns efeitos adversos como por exemplo: alteração da coloração dentária, de restaurações, próteses e língua, formação de cálculo supragengival, perda do paladar, xerostomia e gosto residual desagradável na boca.6
Os óleos essenciais (EO) são misturas complexas de substâncias hidrofóbicas que permitem a rutura das membranas celulares das bactérias e inibem a atividade enzimática das mesmas.7 Os elixires convencionais de óleos essenciais contêm etanol, utilizado para dissolver várias substâncias dos bochechos. Através deste seu mecanismo de ação os elixires com óleos essenciais são considerados muito eficazes no controlo do biofilme, proporcionando um benefício adicional em relação ao controlo da placa bacteriana, quando comparado somente com a escovagem e o uso do fio dentário.8 Atualmente são discutidos vários aspetos relacionados com os efeitos negativos do uso de álcool em elixires orais, como por exemplo o cancro da orofaringe. Apesar de não existir nenhuma evidência científica de que os elixires com álcool provoquem cancro na orofaringe, tentou‑se eliminar o etanol dos elixires orais e procuraram‑se novas fórmulas.9
Recentemente foram introduzidos no mercado os óleos essenciais sem álcool. Sabe‑se que, apesar de parecer não existirem tantos efeitos colaterais na sua utilização, os óleos essenciais sem álcool parecem ser menos eficazes no controlo da placa bacteriana.9
O cloreto de cetilpiridínio (CPC) pode interagir com a membrana celular bacteriana, resultando na perda de componentes celulares, alteração do metabolismo, inibição do crescimento celular e consequente morte celular,10 mantendo a sua substantividade por períodos de três horas.1 O seu uso prolongado pode provocar manchas nos dentes.10 Apesar da escassa evidência científica, a utilização de colutórios contendo CPC como complemento de formas mecânicas de higiene oral, tem sido descrita como benéfica no controlo da placa bacteriana.10
Este estudo tem como objetivo avaliar o efeito anti‑placa de um bochecho de óleo essencial sem álcool e um bochecho de cloreto de cetilpiridínio, em comparação com um controlo positivo de clorohexidina, utilizando um modelo in vivo de crescimento de placa bacteriana durante três dias, assim como testar a hipótese nula de que não haveria diferença entre os três colutórios testados.
Materiais e métodos
Este estudo é um ensaio clínico cruzado, aleatorizado e cego (Figura 1). A aleatorização pelo grupo de teste e de controlo foi realizada através do programa de computador “random.org”.
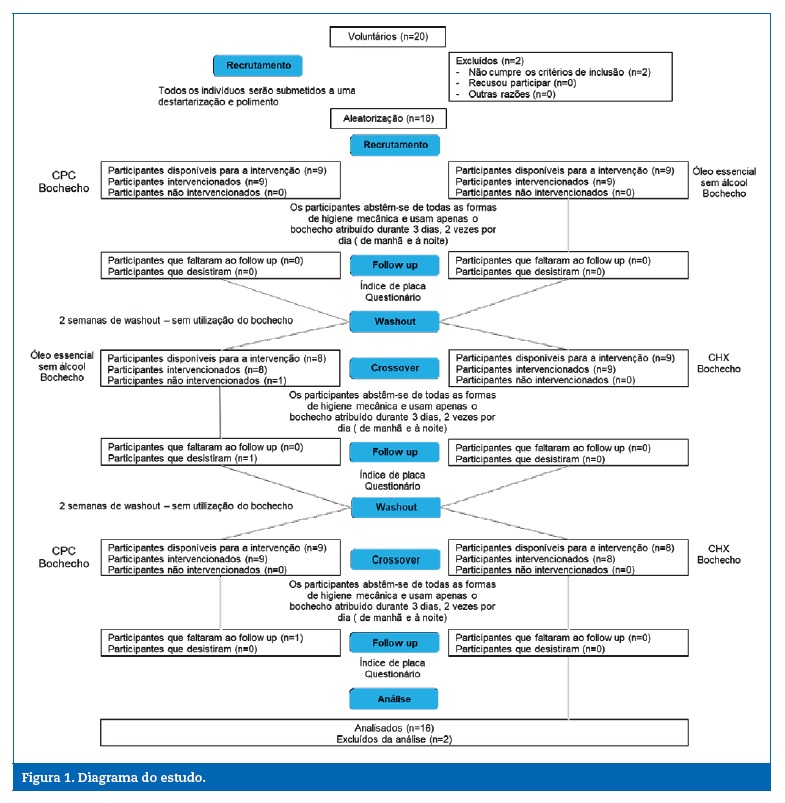
Cada produto foi identificado com um número de um a três eatravés do programa foi decidido, de forma aleatória, qual o produto utilizado por cada participante em cada fase do estudo.
Participaram no estudo 16 voluntários (8 homens e 8 mulheres, entre os 19 e os 21 anos, média de idade de 20 anos).
Os voluntários foram recrutados através de anúncios nas redessociais dos autores. Todos os intervenientes foram seleccionados segundo os critérios de inclusão: boa condição de saúde sistémica, possuir mais de 20 dentes na cavidade oral (mínimo cinco dentes por quadrante), sem lesões orais, sem problemas periodontais graves (sem profundidade de sondagem ≥ 5mm ou perda de inserção> 2mm), sem próteses removíveis ou aparelhos ortodônticos. Foram excluídas do estudo pessoas alérgicas a algum componente dos produtos utilizados. Todos os voluntários que satisfizeram os critérios de inclusão receberam informações orais e escritas sobre os produtos e o propósito do estudo e assinaram um consentimento livre e esclarecido.
O estudo foi realizado de 21 março de 2018 a 3 de Junho de 2018, na Faculdade de Medicina Dentária da Universidade de Lisboa. O protocolo do mesmo foi submetido e aprovado pela Comissão de Ética da Faculdade de Medicina Dentária.
No primeiro dia de cada um dos períodos de estudo, após a verificação dos critérios para inclusão, os voluntários foram submetidos a um exame oral de tecidos moles e duros, seguido de uma destartarização e polimento profissional para a remoção de todo o cálculo existente, manchas extrínsecas e obtenção de um índice de placa de 0. De forma a garantir que todos os depósitos foram removidos uma segunda aplicação de corante foi realizada. De seguida os voluntários foram aleatoriamente distribuídos pelo grupo de teste e de controlo. A ocultação da distribuição foi assegurada. Os participantes do grupo de teste receberam um frasco de bochecho de óleo essencial sem álcool ou cloreto de cetilpiridínio previamente pesado e o grupo de controlo recebeu um frasco com clorohexidina a 0,2% também previamente pesado (Tabela 1). Todos os frascos distribuídos aos intervenientes foram os originais e novos frascos foram utilizados em cada administração. Todos os participantes foram instruídos a não utilizar qualquer outro meio de higiene oral a não ser o bochecho durante o período experimental de três dias e a realizar o bochecho duas vezes ao dia, uma de manhã e outra à noite, com 20 ml de solução, durante 60 segundos, não podendo depois passar a boca por água. Foi ainda entregue a cada voluntário uma folha contendo as instruções do procedimento e a composição de cada produto. O procedimento foi realizado em casa sem supervisão, no entanto, para relembrar e ‘garantir’ a realização do bochecho, os participantes anotaram as horas da realização dos mesmos. Após três dias os voluntários foram examinados com uma solução de eritrosina e a quantidade de placa foi registada em seis locais por dente através do índice Quigley and Hein modificado por Turesky et al e por Lobene et al.11
Todos os frascos de bochecho foram devolvidos nesta altura e pesados para calcular a quantidade de solução utilizada. Os participantes preencheram um questionário com uma escala analógica visual (VAS) de satisfação em relação ao produto utilizado. Os participantes assinalaram um ponto numa linha não calibrada de 10 cm de comprimento com a resposta extrema negativa [0] na extremidade esquerda, sendo a resposta extrema positiva [10] registada na extremidade direita.12

Após esta fase, durante 14 dias (período de washout) os intervenientes voltaram à sua rotina de higiene oral. Passados os 14 dias foram novamente sujeitos a mais uma consulta de higiene oral onde foi realizada uma nova aplicação de corante, destartarização e polimento para obterem índice de placa de 0. O procedimento repetiu‑se, mas, desta vez, com o outro bochecho.
A análise dos dados foi efetuada pelo estudo do valor do índice de placa bacteriana. O estudo da normalidade dos dados foi realizado com o teste de Shapiro‑Wilks.
Para os dados que não possuem distribuição normal foi utilizada a análise de variância não paramétrica (teste de Friedman) para determinar as diferenças entre os produtos testados. Na presença de diferença significativa, a análise post hoc para comparação de pares de tratamento foi realizada usando o teste de postos sinalizados de Wilcoxon com o ajuste de Bonferroni para múltiplas comparações, e a significância para as análises univariadas foi avaliada assim em P<0,0167. Para os dados com distribuição normal, foi utilizada a ANOVA para determinar as diferenças entre os produtos testados, nos casos em que a diferença foi significativa, a análise post hoc para comparação de pares de tratamento utilizada foi a de Tukey. Para a análise estatística foi utilizado um nível de significância de 5%. Os dados recolhidos nos questionários também foram analisados usando os mesmos testes. Os dados foram analisados através do programa IBM SPSS Statistics 25.
Resultados
Todos os participantes (N=16; grupo de 8 CPC; 8 para o grupo de EO sem álcool) completaram o período experimental e não houve valores em falta. As pesagens dos frascos, após a sua utilização, indica que foram utilizados menos do que os 120 ml de solução previstos para os três dias de estudo. A média das pesagens apresenta em média, por cada participante, durante os três dias, 72 ml, 102 ml e 88 ml de solução de CHX, CPC e EO sem álcool, respetivamente. Relativamente aos possíveis efeitos adversos houve cinco relatos de ardor e dormência da língua quer com a utilização do CPC quer com a utilização do EO sem álcool, não existindo nenhuma desistência devido a isso.
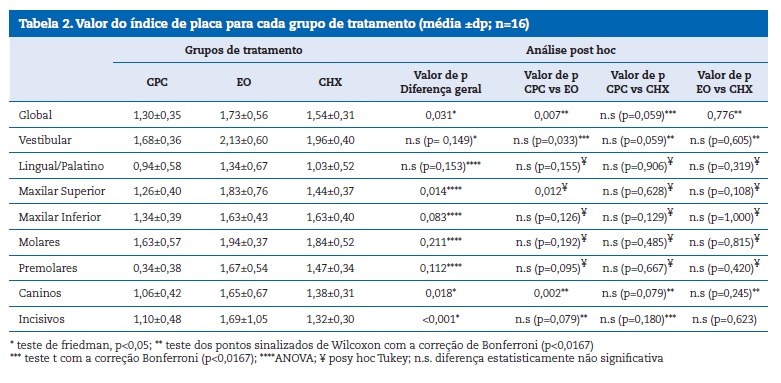
O índice de placa inicial, antes da utilização de qualquer produto, variou entre 0,36 e 2,14. Os valores dos índices de placa dos grupos de teste e de controlo, no final do período experimental, são apresentados na Tabela 2. A análise estatística mostrou a existência de diferenças significativas no índice de placa entre os três grupos. O grupo que utilizou o CPC mostrou um melhor efeito na inibição do crescimento da placa bacteriana quando comparado com o grupo EO. De facto, a média global do índice de placa bacteriana foi menor com a utilização do CPC (1,30) do que com o uso do EO (1,73) e da CHX (1,54). Todos estes valores foram estatisticamente significativos.
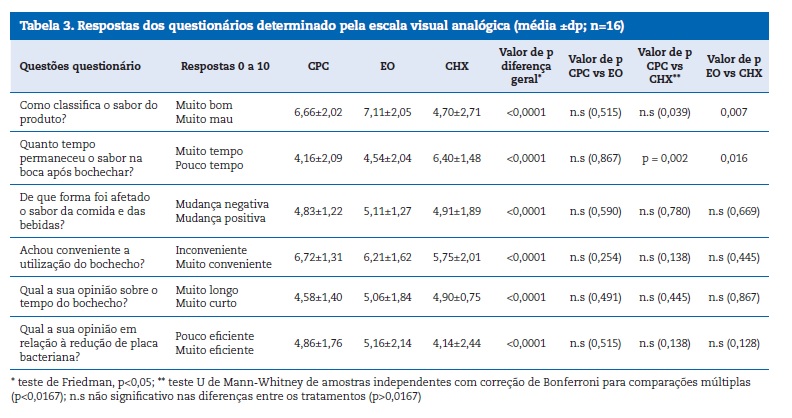
Os resultados obtidos após a análise dos questionários são apresentados na Tabela 3. Em todas as questões do questionário houve diferenças estatisticamente significativas entre todos os produtos utilizados. Os participantes referiram preferir o sabor do CPC (VAS 6,66) e do EO sem álcool (VAS 7,11), em vez do sabor da CHX (VAS 4,70; P<0,0001). No que diz respeito à duração do sabor na boca após a utilização do produto, os indivíduos envolvidos consideraram uma menor duração após o uso do CPC (4,16) e do EO (4,54), do que com a CHX (6,40; P<0,0001). Relativamente à forma como o sabor da comida e das bebidas foi afetado, os voluntários afirmaram a existência de uma mudança mais positiva com EO (5,11) do que com o CPC (4,83) e a CHX (4,91; P<0,0001). Os voluntários consideraram o uso do CPC mais conveniente (6,72) do que o EO sem álcool (6,21) e a CHX (5,75; P<0,0001). No que diz respeito ao tempo do bochecho os indivíduos consideraram o EO mais curto (5,06) do que o CPC (4,58) e a CHX (4,90: P<0,0001).
Por último, em relação à eficácia na redução da placa bacteriana o EO obteve valores mais positivos (5,16) do que os outros dois produtos.
Discussão
A CHX foi utilizada como controlo positivo devido à sua capacidade de reduzir a placa bacteriana em 0,2% 6, 13 e devido às suas propriedades antibacterianas. Em vários estudos já publicados a CHX também foi utilizada como controlo positivo pelas mesmas razões.14
Estudos clínicos controlados de longa duração demostraram efeitos positivos na redução da placa bacteriana supra gengival com o uso do CPC. Em 2008, numa revisão sistemática realizada por Haps et al.15 o uso de colutórios com CPC juntamente com a escovagem apresentou melhores resultados quando comparados com o placebo. No entanto, estes estudos foram realizados a médio e longo prazo, e não a curto prazo como o presente estudo. Num estudo realizado em 2015 por Kang et al.16 concluiu‑se que o CPC apresenta melhores efeitos antimicrobianos quando utilizado em conjunto com o lactado de zinco. No presente estudo foi utilizado um produto à base de CPC com lactato de zinco.
Os EO são considerados muito eficazes no controlo do biofilme, proporcionando um benefício adicional em relação ao controlo da placa bacteriana, quando comparado somente com a escovagem e o uso do fio dentário.8 Marchetti et al.12 num estudo semelhante ao presente trabalho, também testaram a eficácia da inibição de placa bacteriana de um óleo essencial sem álcool, em comparação com um controlo positivo de CHX, durante um período de três dias. Os resultados obtidos nesse estudo foram semelhantes presente estudo, demonstrando um melhor efeito com a CHX.
No presente estudo foi utilizada uma CHX 0.2% com sistema anti coloração (ADS). Existem algumas investigações publicadas sobre o efeito anti placa de CHX com e sem ADS, no entanto os resultados são um pouco controversos. De acordo com Solís et al.18 num estudo publicado em 2011, concluiu‑se não existir diferenças na redução da placa bacteriana entre a utilização de uma CHX 0.2% com ADS e sem ADS. Já num outro estudo publicado em 2012 por Wen et al.19 a CHX sem ADS mostrou um melhor efeito na redução da placa bacteriana do que com o sistema anti coloração.
Vários estudos indicam que a utilização de um colutório com CHX pode levar ao aparecimento de alterações orais como um gosto residual desagradável na boca após a utilização, o que está de acordo com o presente estudo. De facto, dos produtos testados, a CHX foi a que apresentou piores resultados relativamente à questão do sabor. Num estudo semelhante a este, realizado em 2017,12 a CHX, em comparação com um EO sem álcool e um colutório à base de fluoreto de estanho e lactato de zinco, também foi considerada, pelos intervenientes, como apresentando o pior gosto. Este facto pode influenciar fortemente a escolha de um produto na hora da compra, como demonstrado por Cantarelli et al.17 em 2011.
Conclusões
De forma a prevenir o aparecimento de doenças orais, existe cada vez mais interesse em estudar‑se quais as substâncias mais eficazes no controlo da placa bacteriana, a fim de evitar a utilização de mais do que um produto. Através da análise dos resultados foi possível concluir que o CPC apresentou melhores resultados na redução da placa bacteriana, apresentando um índice de 1,30, do que o EO sem álcool e a CHX cujo índice de placa foi de 1,73 e 1,54, respetivamente.
Este estudo pode ter tido como limitações a não supervisão de um profissional aquando da realização dos bochechos em casa, e por isso a sua utilização poderá não ter sido a mais correta. Por outro lado, devido ao curto acompanhamento do paciente, estes resultados poderiam ser considerados preliminares, não podendo excluir a hipótese de que os produtos testados, a médio e a longo prazo, possam ter outros efeitos.
Referências
1. Luís H. Efeito de um elixir com óleos essenciais e um colutório com delmopinol nas bactérias da placa bacteriana. Tese de Doutoramento em Ciências e Tecnologias da Saúde. Faculdade de Medicina Dentária, Universidade de Lisboa, 2010.
2. Lindhe J, Lang NP, Karring T. Tratado de Periodontia Clínica e Implantologia Oral. 5.ª Edição. Rio de Janeiro: Guanabara Koogan. 2010.
3. Gebran MP, Gebert APO. Controle químico e mecânico de placa bacteriana. Tuiuti: Ciência e Cultura. 2004;26:45‑58.
4. Hortense SR, Carvalho ES, Carvalho FS, Silva RPR, Bastos JRM, Bastos RS. Uso da clorexidina como agente preventivo e terapêutico na odontologia. Revista de odontologia da UNICID. 2010;22:178‑84.
5. Najafi MH, Taheri M, Mokhtari MR, Forouzanfar A, Farazi F, Mirzaee M., Comparative study of 0.2% and 0.12% digluconate chlorhexidine mouth rinses on the level of dental staining and gingival indices. Dental Research Journal. 2012;9:305-8.
6. Pegoraro J, Silvestri L, Cara G, Stefenon L, Mozzini CB. Efeitos adversos do gluconato de clorexidina a 0,12%. Journal Oral Investigations. 2014;3:33‑7.
7. Oliveira MAC, Borges AC, Brighenti FL, Salvador ML, Gontijo AVL, Koga‑Ito CY. Cymbopogon citratus essential oil: effect on polymicrobial caries‑related biofilm with low cytotoxicity. Braz Oral Res 2017;31:1‑12.
8. Serbiak B, Fourre T, Geonnotti AR, Gamboji RJ. In Vitro Efficacy of Essential Oil Mouthrinse versus Dentifrices. J Dent. 2018;69:49‑54.
9. Marchetti E, Mummolo S, Mattia JD, Casalena F, Martino SD, Mattei A. Efficacy of essential oil mouthwash with and without alcohol: a 3‑Day plaque accumulation model. Trials. 2011;15;12:262.
10. Alves, D., Costa, A. L., Almeida, R. F., Carvalho, J. F. C., & Felino, A. Cloreto de cetilpiridínio – revisão da literatura. Rev Port Estomatol Cir Maxilofac. 2012;53:181‑9.
11. Cugini M, Thompson M, Warren PR. Correlations Between Two Plaque Indices in Assessment of Toothbrush Effectiveness. J Contemp Dent Pract. 2006;1;7:1‑9.
12. Marchetti E, Casalena F, Capestro A, Tecco S, Mattei A, Marzo G. Efficacy of two mouthwashes on 3‑day supragingival plaque regrowth: a randomized crossover clinical trial. Int J Dent Hyg. 2017;15:73‑80.
13. Reddy R, Palaparthy R, Durvasula S, Koppolu P, Elkhatat E, Assiri KAR. Gingivitis and plaque prevention using three commercially available dentifrices: A comparative clinical and microbiological randomized control parallel study. Int J Pharm Investig. 2017;7:111‑8.
14. Pinho CB. Óleos Essenciais – Listerine®: Uma revisão crítica. Trabalho para obtenção de grau de Especialista em Periodontia. Escola Bahiana de Medicina e Saúde Pública, Salvador, 2012.
15. Haps S, Slot DE, Berchier CE, Van der Weijden GA. The effect of cetylpyridinium chloride‐containing mouth rinses as adjuncts to toothbrushing on plaque and parameters of gingival inflammation: a systematic review. Int J Dent Hyg. 2008;6:290‑303.
16. Kang JH, Jang YJ, Kim DJ, Park JW. Antimicrobial Effectiveness of Cetylpyridinium Chloride and Zinc Chloride – Containing Mouthrinses on Bacteria of Halitosis and Peri‑implant Disease. The International Journal of Oral and Maxillofacial . 2015;30:1341‑7.
17. Cantarelli, R. Perfil de uso de colutórios utilizados pelos pacientes da faculdade de odontologia da Universidade Federal do Rio Grande do Sul. Trabalho final para obtenção de grau de cirurgião dentista. Porto Alegre, 2010.
18. Solís C, Santos A, Nart J, Violant D. 0.2% Chlorhexidine Mouthwash With an Antidiscoloration System Versus 0.2% Chlorhexidine Mouthwash: A Prospective Clinical Comparative Study. J Periodontol. 2011;82:80‑5.
19. Wen L. The effect of chlorhexidine (CHX) with or without an anti‑discoloration system (ADS) on the development of experimental gingivitis in man. Tese de Mestrado em Cirurgia Oral. The University of Hong Kong, Hong Kong, 2012.
Henrique Soares Luis
Correio eletronico: henrique.luis@fmd.ulisboa.pt
Responsabilidades éticas
Proteção de pessoas e animais. Os autores declaram que para esta investigação não se realizaram experiências em seres humanos e/ou animais.
Confidencialidade dos dados. Os autores declaram ter seguido os protocolos do seu centro de trabalho acerca da publicação dos dados de pacientes.
Direito à privacidade e consentimento escrito. Os autores declaram ter recebido consentimento escrito dos pacientes e/ou sujeitos mencionados no artigo. O autor para correspondência está na posse deste documento.
Conflitos de interesse
Os autores declaram não ter conflitos de interesse.
Historial do artigo:
Recebido a 27 de setembro de 2018
Aceite a 27 de dezembro de 2018
On-line a 29 de janeiro de 2019
